ویژگیها و ساختار اسیدهای آمینه

اسیدهای آمینه معمولاً یک ساختار عمومی دارند از این نظر که همه آنها دارای یک اتم کربن آلفا (1)) هستند که به آن یک گروه کربوکسیلیک ،اسید یک گروه آمینی و یک اتم هیدروژن به طور کووالانسی باند شده است ،بعلاوه اتم کربن آلفا به یک گروه شیمیایی خاص یعنی R زنجیره (جانبی) باند میشود که هر کدام از ۲۰ اسید آمینه رایج مورد خاص خود را دارند یک اسید آمینه در محلول آبی هیدرولیز شده و به صورت یون در میآید در این هنگام در pH حدود ،، گروه آلفا-آمینو (a amino) پروتونیزه شده و به شکل یون آمونیومی میباشد در حالی که گروه اسید کربوکسیلیک در حالت غیر پروتونیزه یا شکل یون کربوکسیلات میباشد.
اسیدهای آمینه از نظر رفتار و خواص و همچنین وظایف بیولوژیکی در بین دیگر مواد طبیعی بینظیر میباشند آنها محلول در آب بوده و الکترولیتهای آمفوتریک هستند و در pH های مختلف به عنوان بافر عمل می کنند , یعنی توانایی هر دو نمکهای اسیدی و نمکهای بازی را دارند. اسیدهای آمینه دارای یونهای دو قطبی بوده و ظرفیت قابل ملاحظه جهت افزایش ضریب دی۔ الکتریک محلول محیطی که در آن حل میشوند دارند. آنها ترکیباتی هستند که دارای گروههای فعال یا واکنشگر میباشند که قادرند تغییرات شیمیایی را باعث شوند و به سادگی تولید انواع محصولات تجزیه ای ،سنتزی و محصولات حاصل از تغییر شکل می کنند. این محصولات حاصل از تغییر شکل شامل ،استرها ،آمیدها ،آمینها ،آنهیدریدها ،پلیمرها ، پلیپپتیدها هیدروکسی اسیدها کتواسیدها مرکاپتانها و شکلهای حلقه ای پیرولیدین و پیپریدین و بسیاری مواد دیگر میباشند. اسیدهای آمینه و پروتئین ها جزء اصلی انواع غذاهای جانوران از جمله انسان میباشند در که حیات به آنها بستگی دارد شرکت میکنند و به عنوان سابستریت واکنشهای متابولیکی مهمی برای انواعی از آنزیمها نیز مطرح می باشند.
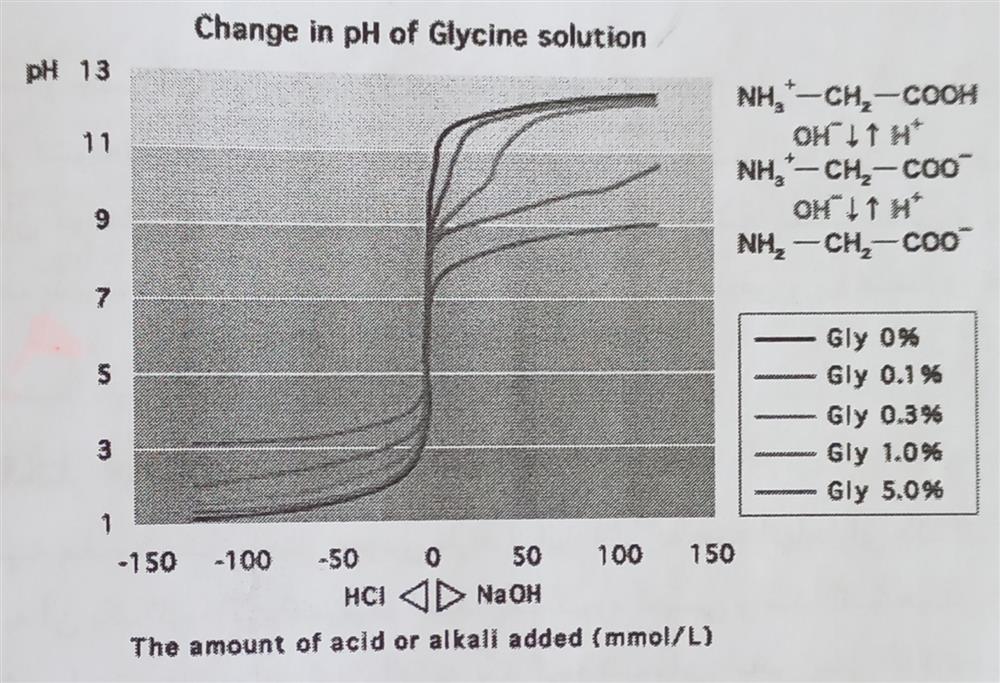
شکل -۳۴ تغییرات pH محلول در اثر اضافه کردن مقادیر گلیسین گلیسین ویژگی بافری مناسبی در مقادیر pH برابر ۲ تا ۳ و pH برابر ۱۰-۹ دارد.
همچنین اسیدهای آمینه و پروتئین ها در دامنه های خاصی از طول موج جذب کننده تابش های ماوراء بنفش و مادون قرمز میباشند این ویژگی باعث میشود که در محافظت اجزای سلولی مانند غشاها و DNA نقش موثری داشته باشند آنها اجزای ضروری مولکول های پروتئین ها هستند که خواص بیولوژیکی و شیمیایی آنها تا حدی بوسیله ،تعداد توزیع و روابط فضایی اسیدهای آمینه ای که آنها را تشکیل میدهند تعین می شود . در یک زمان واحد آنها ممکن است ،تنوع و یا همشکلی را نشان دهند.
همشکلی از آن جهت که با استثناهای بسیار کمی همه آنها اسید آمینه نوع الفا هستند و ویژگیهای فیزیکی که از این واقعیت و تشابه منشاء می،گیرد و اینکه آنها از اجزاء پروتئین و لذا بافتهای زنده می باشند و همچنین همه آنها شکل اپتیکی مشابهی در کرین آلفا دارند.
تمام اسیدهای آمینه موادی آمفوتر هستند یعنی دارای هم گروه هایی با بار مثبت و هم گروه هایی با بار منفی (COOH و NH2 می باشند. این گروه ها به منظور تشکیل پیوندهای پیتیدی با هم ترکیب می شوند تجزیه آنها می تواند تولید مواد زیر کند:
گروه های اسیدی می توانند پروتون های خود را از دست داده و دارای بار منفی شوند چنین تفکیکی در اسیدهای آمینه دارای دو عامل کربوکسیل مثل اسید آسپارتیک و اسید گلوتامیک وجود دارد که گروه کربوکسیل آزاد آن به صورت H و COO- تجزیه میشود.
گروههای بازی با کسب پروتونها دارای بار مثبت میشوند (H) و (NH) که چنین وضعی در اسیدهای آمینه دارای دو گروه بازی مثل ،لیزین یا آرژنین صورت میگیرد که در آنها گروههای آمینه آزاد میتوانند دارای بار مثبت شوند. تمام این عوامل یون ساز و نیز عوامل کربوکسیل یا آمین آزاد انتهایی به پروتئین ها خصوصیات الکتریکی مشخص و امکان انجام واکنشهای اسید باز را میدهد.
در اسیدهای آمینه و پروتئین ها pH اثر شدیدی بر بار الکتریکی کلی مولکول دارد در محیط اسیدی گروههای امینی یونهای هیدروژن را جذب کرده و سپس به صورت باز عمل میکنند. برعکس در محیط ،قلیایی گروه های کربوکسیل تفکیک میشوند. و پروتونها را در محیط آزاد میکنند این در حالی است که هر پروتئین نقطه ایزوالکتریک خاص خود را دارد و این ببرابر PHی است که در آن جمع بارهای مثبت و منفی برابر صفر است.
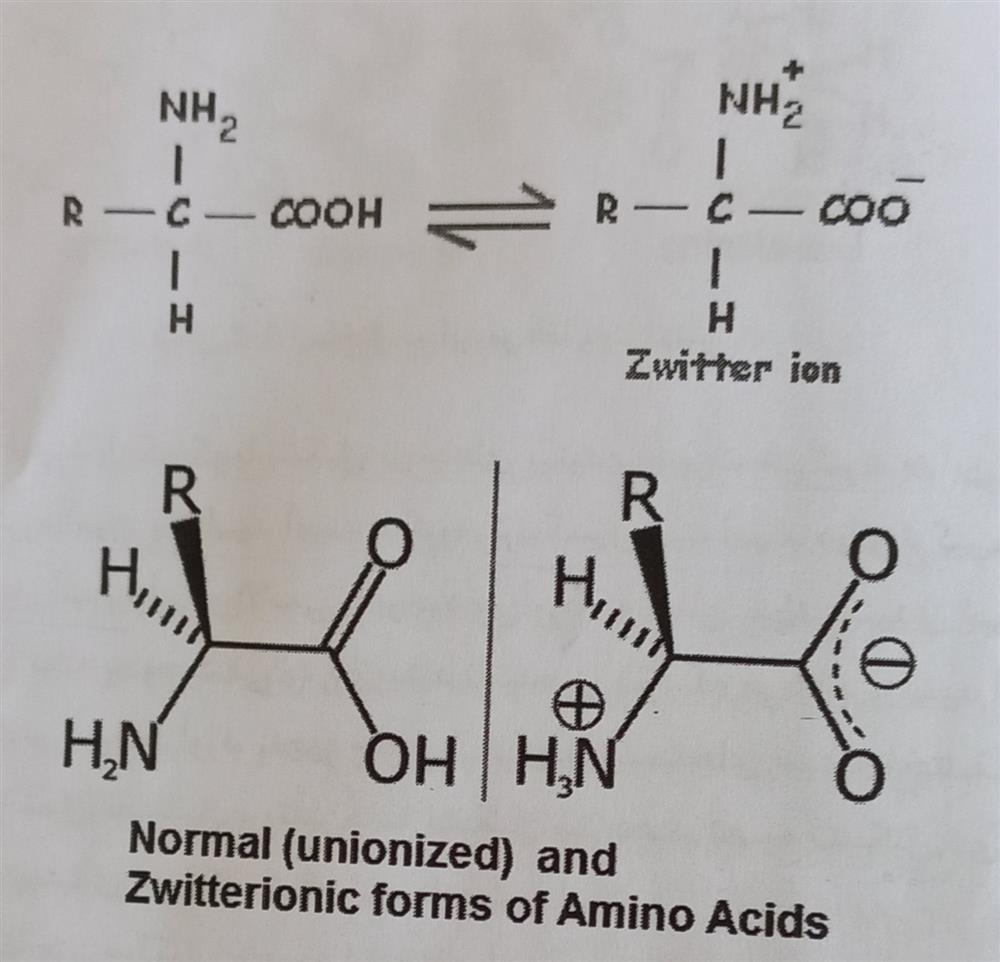
شکل -۴-۴- رفتار اسیدهای آمینه در محیط بازی و اسیدی
همه اسیدهای آمینه بجز گلیسین دارای یک کربن نامتقارن هستند و بنابراین نور پلاریزه را به طرف راست یا چپ منحرف میکنند بر حسب قرارداد در مقایسه با ساختمان فضایی آلدئید گلیسیریک، اگر عامل در سمت راست کربن آلفا باشد اسید آمینه را از نوع (D) و چنانچه در سمت چپ باشد آن را از نوع L مینامند. پروتئین ها پلیمرهای از اسید آمینههای نوع آلفا هستند و تمام اسیدهای آمینه موجود در ساختمان پروتئینهای سلولی از نوع هستند آلفا و بتا اشاره به نوع کربنی است که گروه آمینی به آن متصل می باشد. ساختار آلفا و بتا آلانین در شکل ۵۴ نشان داده شده است. علاوه بر ۲۰ اسید آمینه طبیعی ۱۵۰ اسید آمینه دیگر نیز در سیستمهای زنده یافت میشوند که در ساختمان پروتئین ها شرکت ندارند و آنها را اسید آمینه های غیر پروتئینی مینامند. این اسیدهای آمینه گاهی به صورت ترکیب در جانداران یافت میشوند که آنها را تحت عنوان فرمهای بتا (B) و آلفا (a) و گاما (Y) و دلتا (6) نیز مینامند به عنوان مثال ،آلانین زیربنای ساختمانی اسید پنتاتونیک است هوموسیستئین و هوموسرین واسطه های متابولیسم سایر اسیدهای آمینه اند. D-آلانین در لاروها و شفیره های بعضی حشرات -D گلوتامیک اسید در دیواره باکتریها و D سرین در کرم خاکی را میتوان نام برد
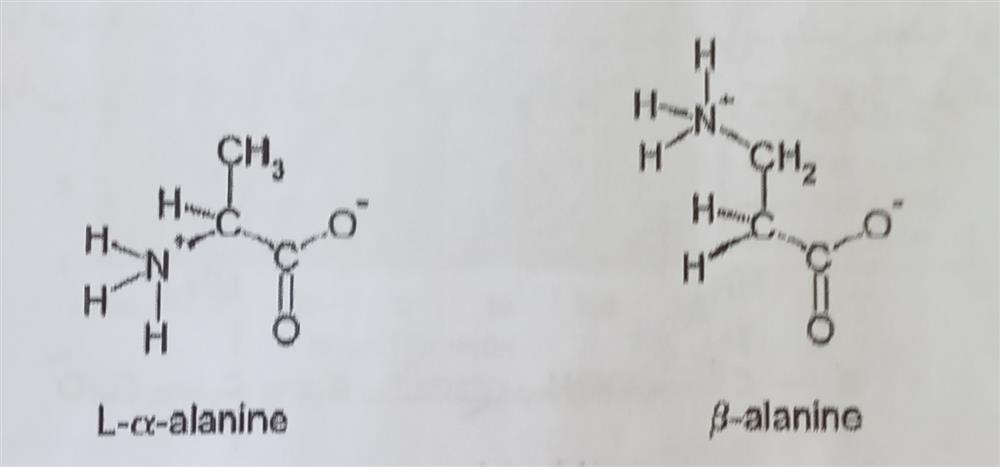 شکل -۴-۵ ساختار دو ایزومر آلفا و بتا آلانین
شکل -۴-۵ ساختار دو ایزومر آلفا و بتا آلانین
ترکیب اسیدهای آمینه با یکدیگر با تشکیل پیوندهای پپتیدی صورت میگیرد به این ترتیب که در طی سنتز پروتئین گروه آمین یک اسید آمینه با گروه کربوکسیل اسیدآمینه دیگر ترکیب شده و با از دست دادن یک مولکول آب پیوند کووالانسی را بوجود می اورد که همان پیوند پتیدی است. مولکولی که از ترکیب دو اسید آمینه به وجود میآید دی پپتید نامیده میشود که میتواند با اسید آمینه دیگری ترکیب شده و تری پپتید را بوجود آورد زنجیر حاصل از ترکیب اسیدهای آمینه مختلف پلی پپتید نامیده میشود که ساختمان نخستین پروتئین ها را تشکیل میدهد نحوه تشکیل دی پپتید از دو اسید آمینه بوسیله باند پپتیدی در شکل ۶۴ نشان داده شده است. بر حسب قرارداد اگر وزن مولکولی مجموع اسیدهای آمینه در مولکول از ۵۰۰۰ دالتون تجاوز نکند مولکول را پپتید یا پلی پپتید و در حد بیش از ۵۰۰۰ دالتون مولکول را پروتئین مینامند فاصله اتصالهای پپتیدی حدود ۳/۵ آنگستروم است . یک پروتئین با وزن مولکولی ۳۰۰۰۰ دالتون و دارای ۳۰۰ اسید آمینه اگر به طور کامل کشیده باشد طولی حدود ۱۰۰۰ آنگستروم و عرضی معادل ۱۰ آنگستروم و ضخامتی حدود ۶-۴ آنگستروم خواهد داشت.
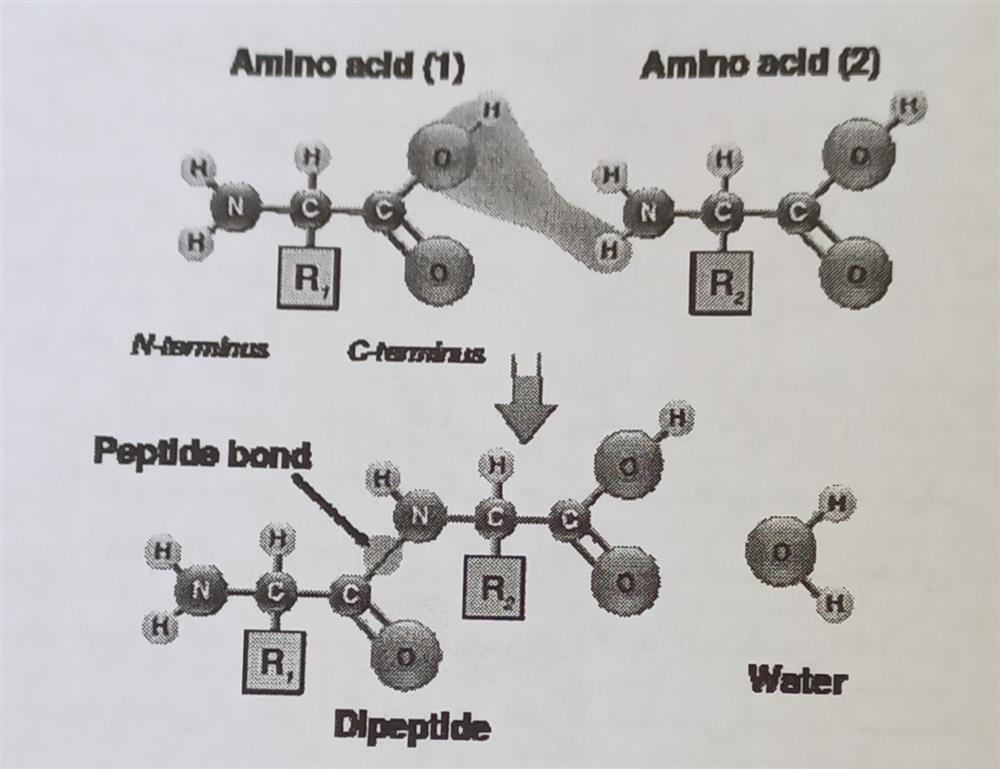 شکل -۴-۶- نحوه باند شدن دو اسیدآمینه و تشکیل پپتید
شکل -۴-۶- نحوه باند شدن دو اسیدآمینه و تشکیل پپتید
اسیدهای آمینه به عنوان باند کننده بسیاری از فلزات نیز مطرح هستند و این مهمترین ویژگی آنها از منظر این کتاب میباشد قابلیت اسیدهای آمینه جهت تشکیل کمپلکس های فلزی نه تنها از نظر تئوریکی مهم است بلکه در عمل نیز اهمیت زیادی دارد تولید مکملهای تغذیه ای عناصر غذایی مانند ،روی ،آهن ،مس پتاسیم و کلسیم چندین دهه است که برای رفع کمبودهای عناصر در انسان تولید و تجویز می شوند. از این نظر شاید سابقه تولید کمپلکس های عناصر با اسیدهای آمینه به کارهای هوف مایستر و ورنر بر می گردد به هر حال ترکیبات فلزی گلایسین و دیگر اسیدهای آمینه اولین بار توسط Ley طی سالهای ۱۹۰۴ تا ۱۹۰۹ تولید شدند تولید مکملهای غذایی برای گیاهان یا کودهایی بر اساس اسیدهای آمینه تنها در سالهای اخیر به صورت تجاری صورت گرفته است این شکل کودها می توانند نقش مهمی در کاهش آلودگیهای محیطی ناشی از کاربرد کودها داشته باشند، چرا که اغلب کارآیی بالاتری داشته و برای پاسخی مشخص به مقدار کمتری از این کودها نیاز است.
اسیدهای آمینه ماهیتی آمفوتریک دارند و این ویژگی باعث میشود که این ترکیبات بتوانند با اسیدها و بازها واکنش کنند اسید آمینههایی که حاوی بیش از یک گروه بازی هستند تمایل بیشتری برای واکنش با اسیدها .دارند لذا هیستیدین و لیزین میتوانند به ترتیب تشکیل هر دو نمکهای اسید مونوهیدروکلریک و دی هیدروکلریک نمایند.
در یک محلول آبی در حضور اسیدهای آمینه و قندهای احیا ،شونده واکنشی بین آنها ممکن است رخ دهد و مخلوط آنها به آهستگی قهوه ای رنگ میشود این تغییر رنگ مربوط به تشکیل -N گلوکوزیدها میباشد که ترکیبات این چنینی به راحتی در pH خنثی یا اسیدی به محصولات اولیه هیدرولیز میشوند.

